|
La Glande labiosternale des Theridiosomatidae ANATOMIE DES ARAIGNEES : VINGT-CINQ ANS DE RECHERCHES Par André LOPEZ, auteur (version 2024) |
Un curieux organe glandulaire ventral dans le céphalothorax des Theridiosomatides, petite famille d' Araignées dont il est hautement caractéristique |
|
1- Introduction
2- Organe labiosternal
2.1 - Pore labiosternal
2.2- Structure histologique
2.3 -Ultrastructure
2.3.1.a -Adénocyte
2.3.1.b -Appareil cuticulaire individuel3-Commentaires
La glande
labiosternale
est un organe sécréteur exocrine qui semble
propre aux seuls Theridiosomatidae, petite famille
d’ Araignées “ Labidognathes ”, pour la plupart
tropicales, se rattachant aux
Araneoidea les plus primitives
et dont la biologie parait
encore
mal connue (Coddington,1986).
L'auteur en a décrit trois
espèces
sud-américaines : Wendilgarda
mustelina arnouxi Lopez,1985
(Guadeloupe)
; Ogulnius
hayoti Lopez,1994 (Martinique) ; Plato
juberthiei Lopez,1996
(Guyane).
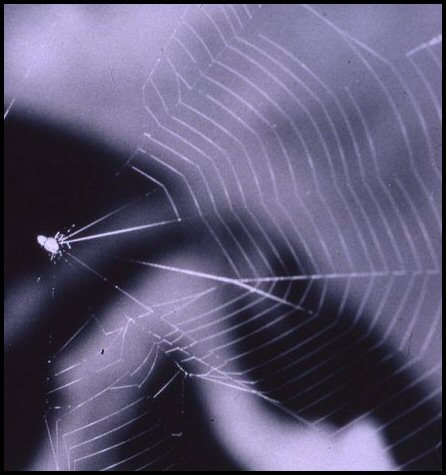
Selon les
genres, elles construisent dans les lieux humides des toiles d’aspect
variable, les
unes rudimentaires (Wendilgarda), les autres
plus élaborées, tenues sous tension et
étirées en cône formant pièges à
ressort (Theridiosoma,
Naatlo)(Fig.1).
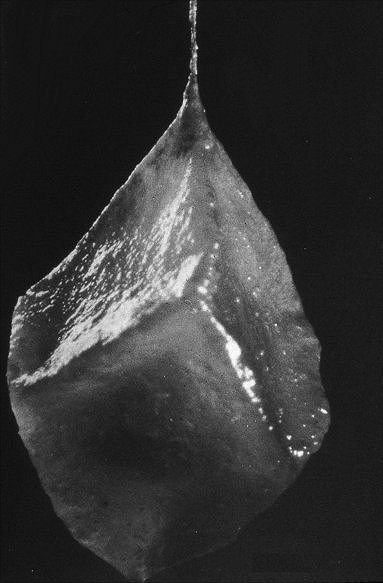
De
plus, elles tissent des cocons ovigères
pouvant présenter une forme cubique trés
curieuse, apparemmernt unique
dans l'ordre des Araneides
(Fig.2,3), par ailleurs modèle
géométrique rarissime dans le
monde animal.
 |
 |
 |
| Fig.1
Naatlo
splendida sur sa toile |
Fig.2-
Wendilgarda sp. |
Fig.3 - Plato juberthiei |
| Forêt du Rorota, Rémire-Montjoly, Guyane (© photo A.Lopez) | Cocons
ovigères cubiques (© A.Lopez M.E.B.) |
|
Dans leurs
études morphologiques de Wendilgarda
américaines, Archer (1953) et Brignoli
(1972) ont signalé l’existence de petites
“ fossettes sternales"
(“sternal pits ”)
rapprochées du labium,
retrouvées
plus tard par Wunderlich
(1980) (“ sternal-organ ”) chez d’autres genres de
Theridiosomatidae (Theridiosoma, Ogulnius, Epeirotypus) et
qu’il considère comme une
autapomorphie
familiale.
Ultérieurement encore, Coddington
(1986) les signale
comme caractères de diagnostic dans sa monographie sur tous les
genres connus de Theridiosomatidae.
Wunderlich
(1980) a précisé,
que
les “ organes sternaux ” ont l’ aspect d’ invaginations
sacciformes, de nature glandulaire, mais il s’est uniquement
basé sur l’examen superficiel et grossier
de préparations éclaircies, sans exploration
consécutive (Note 2)
L'auteur
a réalisé les
premières
études histologiques et ultrastructurales jamais
effectuées sur l’ “organe sternal”(Lopez,1983a
; Lopez,1988
; Lopez,1993c) apportant
ainsi la preuve
formelle qu’il est de nature glandulaire et s’ouvre bien à
l’extérieur par la fossette
(“pit”). Il a également
proposé d’appeler cette dernière “ pore
labio-sternal ” et
la
structure qui y débouche,
“ organe
labio-sternal ”,
ces noms
composés exprimant mieux
leur position très antérieure au contact du labium.
Le
matériel étudié se compose de 3 Theridiosomatidae
néotropicaux
: Wendilgarda
mustelina arnouxi Lopez,1985
(Guadeloupe), Theridiosoma sp.
(Martinique) et Naatlo
splendida ex Theridiosoma splendidum
Taczanowski
(Guyane française) ( Note 1)
2 - Organe labio-sternal
2.1-Pore labio-sternal
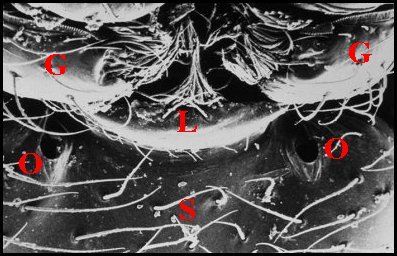
Vu au
M.E.B., il se présente comme un
orifice régulier située
sur le sternum
au contact de
son bord
antérieur et de l’extrémité du labium, donc
de la suture labio-sternale,
régulière,
ovalaire et bordée d’une petite margelle postérieure chez
Wendilgarda mustelina
arnouxi
Lopez
& Emerit 1985 de Guadeloupe (Fig.4,5) à peu
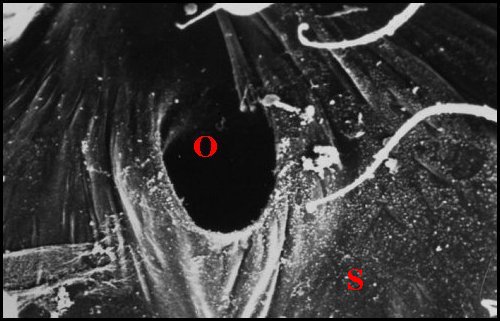
prés circulaire et de niveau avec la surface du tégument
chez
Theridiosoma sp, de
Martinique (Fig.6), regardant
obliquement en bas, en avant et un peu en dedans, mesurant de 10
à 20 µm de diamètre.
 |
 |
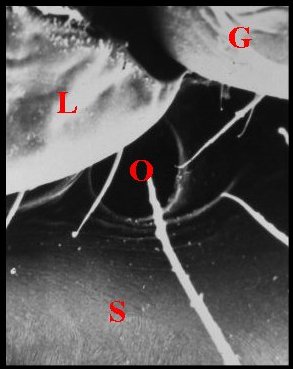
| Fig.4 - Wendilgarda mustelina arnouxi : région labio-sternale | Fig.5
- Pore
labio-sternal, détail de la précédente |
| G, gnathocoxae - L, labium - O, pores labio-sternaux - S, sternum (© A.Lopez M.E.B.) | |
 |
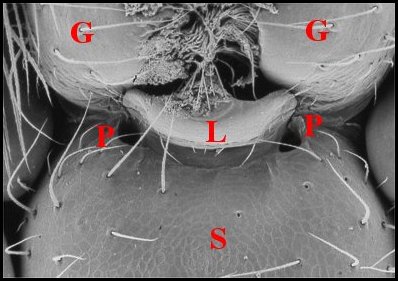 |
| Fig.6 - Theridiosoma sp., pore, détail | Fig.7 - Plato juberthiei : région labio-sternale |
| G, gnathocoxae - L, labium - 0,P, pores labio-sternaux -S, sternum (© A.Lopez M.E.B.) | |
Cet
aspect se retrouve chez d’autres Theridiosomatidae tels que Plato
juberthiei Lopez
1996a de
Guyane (Fig.7), et Ogulnius
hayoti Lopez,1994
de Martinique.
L’organe s’abouchant au pore est pair, symétrique, paramédian, superficiel et repose sur le tégument sternal au voisinage immédiat du labium. Recouvert par la masse nerveuse sous-oesophagienne, il est constitué par un massif glandulaire et une poche réceptrice commune (Fig.8,9).
Ainsi que l’indiquait Wunderlich (1980)
d’après ses préparations éclaircies, cette poche
est un “ sac ” s’ouvrant extérieurement au niveau du
pore labio-sternal,
allongé (L = 90 à 100µm),
plus large dans sa moitié postérieure (l = 60 à 70
µm) que dans l’antérieure (l = 40 µm), donc
ovoïde ou piriforme (Fig.8,9) et orienté de telle
sorte que son grand axe est à peu prés horizontal,
égèrement oblique en avant et un peu en dedans.
Sa
paroi est formée par une
assise
épidermique fine, bien visible seulement
lorsqu’elle contient un pigment noir et
surtout, par de la cuticule.
Cette
dernière,
très
mince au niveau du fond ou globalement chez
Naatlo (2 µm),
s’épaissit
progressivement dans la partie antérieure (Wendilgarda)
où elle atteint 4 µm et se
raccorde à la chitine
sterno-labiale (10 µm) sur le pourtour
du pore
(Fig.5).
Ainsi se présente-t-elle
comme une invagination en profond récessus du tégument et
repose sur ce dernier par sa face ventrale
sans lui adhérer.
 |
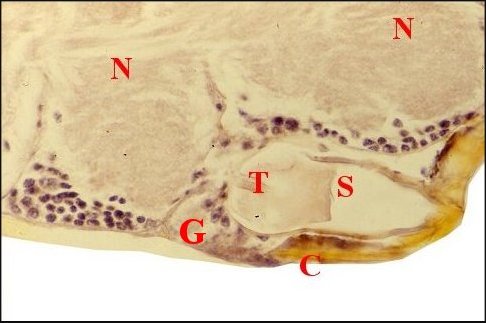 |
| Fig.8 - Wendilgarda mustelina arnouxi : coupe passant par le pore. | Fig.9 - Wendilgarda mustelina arnouxi, coupe passant en dehors du pore. |
| C, cuticule ventrale - G, massif glandulaire - H, poils - N, ganglions nerveux - P, pore - S, sécrétion - T, "tigelle" (© A.Lopez C.H.) | |
La cavité ou
lumière de la poche renferme un matériel
amorphe
éosinophile en boules et masses irrégulières. Chez
Wendilgarda (Fig.9 à
11), il englobe de curieuses saillies
pariétales,
sorte de “ tigelles ”
cuticulaires se détachant sur
le pourtour du fond, longues en moyenne de 15 µm, bi ou
trifurquées à leur extrémité libre et s’y
terminant en pointes plus ou moins
divergentes (Fig.10 ). Elles sont remplacées
par de simples “ dentelures ” postérieures chez Naatlo.
 |
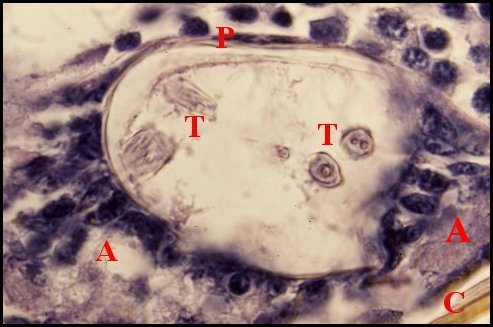 |
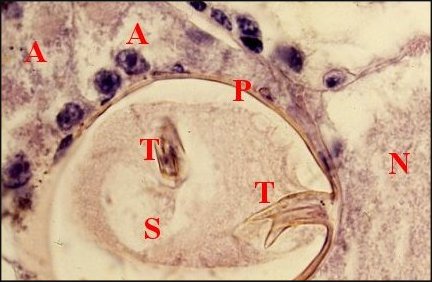
| Fig.10 - Wendilgarda mustelina arnouxi, coupe transversale | Fig.11 - Wendilgarda mustelina arnouxi, autre coupe transversale |
| A,
adénocytes - N, ganglion nerveux - P, paroi de la poche -
S,
sécrétion - T, "tigelles" (© A.Lopez C.H.) |
|
Le
massif
glandulaire s’inscrit toujours dans
une loge en triangle, haute d’environ 30 µm, que
délimitent le pôle postérieur de la poche, les
ganglions sous-oesophagiens et
le tégument
sternal. Ce massif
est très compact chez Wendilgarda
et Naatlo,
ne dépassant pas vers l’arrière le niveau du ganglion de
P
II. Par contre, il est moins
dense chez Theridiosoma, y
adoptant une disposition en chapelet qui
atteint le ganglion de P III.
Il se compose de cellules
ayant
un aspect sécréteur, donc d'adénocytes, et de
canalicules excréteurs
flanqués par des cellules
“ satellites ”. Les adénocytes
sont
volumineux (30 µm), oblongs, pourvus
d’un noyau arrondi
vésiculeux ( 8 à 10
µm), nettement nucléolé ; leur cytoplasme
est basophile en
périphérie et présente une zone centrale
éosinophile, striée, de forme ovalaire, évoquant
un “ réservoir ”
où débute
un très grêle canalicule
également coloré
par
l’éosine. Les cellules
“ satellites ”
siègent entre les adénocytes
et la paroi de la poche, ont
un
petit noyau allongé
(4 µm),
à chromatine
abondante,
un cytoplasme pâle
peu visible et
entourent les canalicules
venant
de se dégager des
adénocytes.
Ces conduits sont
grêles, tortueux,
convergent vers la paroi de la poche
et la traversent en une zone
limitée de son
pôle postérieur, au niveau
des dentelures.
L’étude
ultrastructurale chez Naatlo et Wendilgarda (Lopez,1988 ; Lopez,1993)
montre que les cellules et les
canaux sont bien réunis
en unités
glandulaires fonctionnelles
toutes semblables (Schémas 1 et 2) dont la
sécrétion est
reçue par la poche
collectrice. Cette
dernière et l’ensemble de tous les canaux
qui y aboutissent, récepteurs
inclus, constituent un appareil
cuticulaire
global.
Chez
les deux espèces
étudiées, elle comporte un adénocyte
et la partie de l'appareil
cuticulaire qui le dessert, soit un canalicule récepteur,
un canalicule excréteur ou
conducteur et des cellules
canaliculaires (Schémas
1 et 2).
2.3.1.a
-Adénocyte
Il
se
présente comme une grosse cellule
pyramidale.
Son
pôle
externe ou basal, au
contact du sinus
hémolymphatique, montre
quelques invaginations
de la membrane
(Wendilgarda)(Schéma
1) ou est
régulièrement arrondi, sans indentations
particulières
(Naatlo)(Schéma
2)
En revanche, son
pôle
apical est caractérisé par
une invagination de l’espace
extracellulaire en
“ cul de sac ” ou “ doigt de
gant ”, occupant le grand axe adénocytaire,
légèrement
flexueuse et renferme un canalicule
récepteur en position centrale.
Cette invagination est
bordée par des microvilli
convergeant vers le
canalicule
récepteur, très
nombreuses, longues en moyenne de 3 µm et remarquables par
leur
aspect très particulier. Aplaties en lamelles, elles se
présentent comme des expansions
foliacées beaucoup
plus larges (1 µm) à la base qu’au sommet qui
s’effile
régulièrement en cône allongé.
Elles
ont ainsi un contour à peu prés triangulaire,
parfois cordiforme ou en “ as de pique ” lorsqu’il existe un
léger pincement au-dessus de leur base (Wendilgarda)
(Schéma 1 : 2). En outre, ces microvillosités ne
sont pas planes mais sinueuses,
et plus ou
moins incurvées sur leurs
deux axes. Elles s’appliquent enfin
étroitement les unes contre les autres en
s’imbriquant
(Schémas 1,2 ;
Fig.12,13) et ne ménagent que des
espaces virtuels ou que souligne
un matériel
osmiophile très peu abondant. Cette
juxtaposition dense des microvilli
crée
des images très
particulières dues à l’accolement : “ nids
d’abeille ” lorsqu’elles
sont coupées
transversalement ; bandes tranversales grenues
équidistantes ou festons de zonation régulière
(Fig.12, 15) lorsque leurs coupes sont obliques. Les mêmes
microvillosités
renferment des filaments
intermédiaires (Wendilgarda),
des microtubules
longitudinaux (Naatlo)
s’étendant de la base
à l’apex où
ils se disposent
en couronne, et, dans ce même apex, une petite
densification terminale.
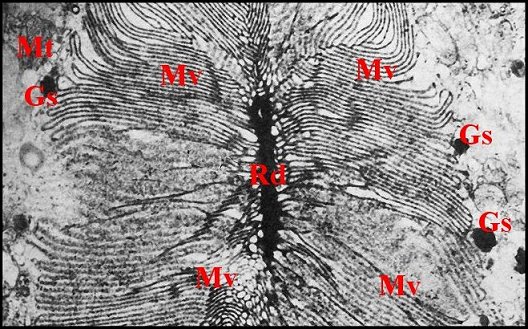 |
 |
|
Fig.12 - Wendilgarda arnouxi : microvilli,
canalicule récepteur
|
Fig. 13 - Wendilgarda arnouxi : microvilli,
grains de sécrétion
|
| Gs, grains de sécrétion- Mt, mitochondries - Mv, microvillosités - Rd, canalicule récepteur (© A.Lopez M.E.T.) | |
Le noyau
siège en
général
dans la partie moyenne de l’adénocyte.
Il est volumineux, clair, arrondi ou
ovoïde et contient un nucléole
réticulé excentrique. Sa chromatine est
abondante,
dispersée dans le nucléoplasme
et forme aussi de petites mottes marginales. L’enveloppe
nucléaire est
en nette continuité avec le réticulum
endoplasmique.
Ce dernier est granulaire ou rugueux. Chez Wendilgarda,
il est
formé par de petits sacs
variqueux, siégeant surtout prés de la cavité
extracellulaire et
en périphérie, tandis que chez
Naatlo, il
paraît plus abondant et se compose de cisternae
allongées, planes ou incurvées, formant par empilement un
ergastoplasme
développé, surtout dans la
périphérie de l’adénocyte
qui leur doit sa basophilie.
Le chondriome est
également remarquable par son
abondance (Fig.15). Il se compose de mitochondries
volumineuses,
à
matrice claire et crêtes sinueuses,
réparties sans ordre
apparent, très plastiques, souvent accolées en amas
compacts et alors déformées par compression
réciproque.
De même, l’appareil
de Golgi ou complexe
golgien est très développé, du
moins chez Wendilgarda. Il
réunit des dictyosomes
nombreux, petits, localisés près de la cavité
extracellulaire,
constitués chacun par un
empilement de 3 à 5
saccules plus ou moins
dilatés, présentant une face
“cis” (proximale ou de formation) en
rapport avec le réticulum
endoplasmique et une face
“trans”
(de sortie ou de maturation) orientant sa concavité vers
l’espace
extracellulaire. Par
cette face et les bords de ses saccules,
chaque dictyosome
bourgeonne un essaim de vésicules
golgiennes recouvertes (réseau
transgolgien), qui grossissent
progressivement et donnent ainsi naissance aux grains de
sécrétion.
Ces grains sont
arrondis ou anguleux, limités par
une membrane et
contiennent un matériel opaque,
d’abord finement grenu, ensuite homogène et très
osmiophile. Ils gagnent la base des replis
microvillositaires, y
émettent de petites protubérances s’abouchant dans les
interstices et libèrent ainsi leur contenu qui s’insinue entre
les microvilli jusqu’ au
canalicule
récepteur.
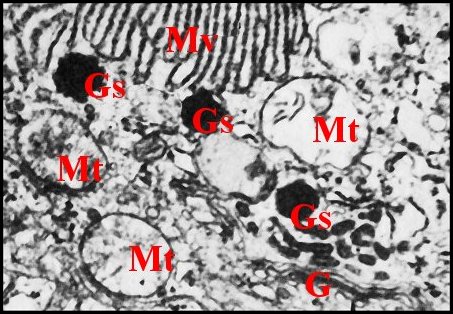
Les autres organites
subcellulaires
sont de petites vésicules
d’endocytose (pinocytose)
entre les microvilli,
des endosomes rejoints
par les précédentes, des
ribosomes libres, des microtubules pouvant s’engager
dans les microvilli,
des microfilaments qui
y pénètrent aussi et des lysosomes secondaires, sans
localisation précise,
plus ou
moins anguleux et à contenu membranaire
hétérogène.
 |
 |
| Fig.
14 - Wendilgarda arnouxi :
organites
sub-cellulaires divers |
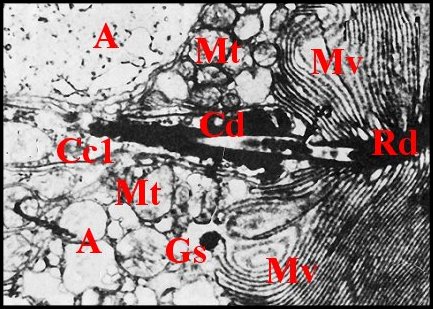
Fig.
15 - Wendilgarda arnouxi :
jonction des
deux canalicules |
| A, adénocytes voisins - Cc1, cellule canalaire proximale - Cd, canalicule conducteur - G, Golgi (dictyosome) - Gs, grains de sécrétion - Mt, mitochondries - Mv, microvillosités - Rd, canalicule récepteur (© A.Lopez M.E.T.) | |
2.3.1.b- Appareil cuticulaire individuel
Drainant
et emmagasinant la sécrétion de chaque adénocyte,
il est
formé par
l’ensemble des canalicules
récepteur et conducteur,
ce dernier, qu'entourent des cellules
canaliculaires, jusqu'à sa
terminaison (orifice) dans la poche
collectrice.
2.3.2.a-
Canaux
Le
canalicule
récepteur est
entièrement logé dans la cavité extracellulaire de
l’adénocyte
et en forme l’axe (Schémas 1 et 2, Fig.12,15). Il
présente une lumière
très étroite, aplatie
(0,3 µm en moyenne) et une paroi
formée par de l’épicuticule
externe, opaque aux
électrons, très mince (10 nm), régulière,
lisse sur ses deux faces, paraissant compacte et homogène chez Naatlo
(Schéma 2),
montrant en fait chez Wendilgarda deux couches discontinues lui
donnant un aspect
fenestré et s’interrompant peut-être aussi vers
l’extrémité distale (Schéma 1-1). A ce
niveau, le canalicule
semble s’ouvrir dans la cavité
extracellulaire, relativement
spacieuse et contenant du
matériel grenu. Partout
ailleurs, le canalicule
est en contact avec les
apex microvillositaires qui s’accolent à lui. Il contient
un
matériel dispersé et finement granuleux ou plus dense,
homogène, très osmiophile semblant mouler la
lumière.
Le
canalicule
conducteur est beaucoup plus
long que le précédent, lui fait suite au niveau de l’apex
adénocytaire, décrit des sinuosités plus ou
moins parallèles à la poche
collectrice (Fig.16), gagne
enfin la paroi
de
cette dernière et s’y ouvre
par un pore excréteur.
Il présente une lumière
arrondie
(D = 0,5 µm), vide ou à contenu osmiopohile granuleux, et
une paroi ininterrompue
formée par deux couches
d’épicuticule,
l’une interne mince,
régulière, lisse du côté de la
lumière, l’autre
externe plus dense, épaissie en
mamelons irréguliers, surtout dans la
partie proximale où ils forment des masses polylobées.
2.3.2.b- Cellules canaliculaires
Il semble n’y en avoir que deux, proximale et
distale,
chez Naatlo splendida
(Schéma
2), cas le plus simple, et un
ensemble plus complexe chez Wendilgarda arnouxi
(Schéma
1) où seules, la première et la dernière
peuvent être encore individualisées.
Elles sont allongées, aplaties et
s’enroulent autour du canalicule
excréteur ou conducteur,
leurs faces accolées formant un méso
plus ou moins sinueux, clos par une zonula adherens.
Le noyau
est
également allongé et déprimé,
irrégulier, anguleux et renferme une chromatine
compacte se condensant en grosses mottes ou blocs marginaux
Le cytoplasme,
clair et
peu abondant, renferme des polysomes, quelques
mitochondries, des microtubules se disposant en
paquets
longitudinaux et ne présente jamais les stigmates d’une
activité sécrétoire.
Dans le cas de Wendilgarda, la cellule toute distale est particulièrement allongée, pénètre avec le canalicule conducteur dans une pointe de "tigette" ("digitation") où son cytoplasme, remontant bien au-delà de l'orifice excréteur (Schéma 1-1), s'y moule étroitement ; il renferme des vésicules de réticulum, des microtubules longitudinaux et des mitochondries de forme parfois complexe (Schéma 1-2, Fig.17).
 |
 |
| Fig. 16 - Wendilgarda arnouxi : canalicule conducteur | Fig.17 - Wendilgarda arnouxi : digitations d'une apophyse |
| Cc2, cellules canaliculaires intermédiaires ; Cd, canalicule conducteur (plusieurs coupes de ses sinuosiotés dans la Fig.16) ; Ch, chambre ou poche collectrice ; Cu, cuticule ; Da, digitation ; Mt, mitochondrie ; N, noyau S, sécrétion. Flèches (Fig. ) : mamelons épicuticulaires (© A.Lopez M.E.T.) | |
2.3.2.c-
Poche collectrice
Sa
paroi est bien
formée par un revêtement
chitineux et par une
assise
épidermique interrompue dans
la zone où aboutissent les
canalicules.
Le
revêtement
chitineux
montre une couche intérieure d’épicuticule
(épicuticule
externe et interne)
en continuité avec la paroi des canaux au
niveau de leurs pores
excréteurs individuels (Schéma 2), et
une couche extérieure d’épicuticule,
plus épaisse, montrant des canaux-poraires (pores-canaux),
stratifiée en unités laminaires,
s’interrompant brusquement au niveau des mêmes orifices. Elles
sont toutes deux en continuité avec celles du tégument
ventral sur le pourtour du pore
labio-sternal. L’endocuticule
tégumentaire qui est d’ailleurs
absente de toute la poche,
s’y
termine en un “coin effilé”.
Dans le cas simple de Naatlo
(Schéma 2),
l’épicuticule interne
s’épaissit irrégulièrement
entre les pores canalaires,
formant des crêtes aiguës ou
émoussées qui correspondent aux dentelures des coupes
histologiques.
Dans celui, plus complexe de Wendilgarda
(Schéma 1), la paroi de la poche s’infléchit
brusquement dans les projections très saillantes qui avaient
l’aspect de “tigettes” en
microscopie photonique mais que nous pouvons
qualifier ici “apophyses”,
un peu incurvées, effectivement
("pointes") à leur extrémité libre et
présentant une section transversale oblongue. Comme le reste de
la paroi, ces apophyses, effectivement bi-
ou tri-furquées en digitations
à leur extrêmité libre (Schéma 1-3),
sont formées par
de l’épicuticule
et une exocuticule plus mince
qu’ailleurs, assez riche en canaux
poraires
renfermant
des languettes cytoplasmiques.
Leur axe est occupé par des cellules épidermiques,
par la cellule
distale du canalicule conducteur (Schéma1-1)et la
terminaison de ce dernier, ouvert en
entonnoir sur le tiers inférieur de l’apophyse, au
niveau de sa concavité (Schéma 1-3).
Le
contenu de la poche est
un
matériel
sécrétoire opaque aux électrons,
intensément osmiophile, amorphe, adhérant chez Wendilgarda
à la paroi
et ses apophyses en
une pellicule discontinue. Il forme surtout des
masses plus ou moins volumineuses et
coalescentes, à contours concaves chez Naatlo ou
sphériques, homogènes ou
criblées de lacunes arrondies, montrant, chez Wendilgarda,
une “écorce” périphérique.
2.3.2.c-
Cellules
épidermiques
Peu
nombreuses, elles se logent entre la cuticule
de la poche et les adénocytes,
s’engrènent par
leurs faces latérales, entourent aussi les cellules canalaires,
leur sont
unies par
de petites jonctions subapicales
(zonula adherens) et ,
dans le cas de Wendilgarda,
pénètrent dans les axes des apophyses, y accompagnant le
canal et sa cellule distale.
Chaque cellule
épidermique montre un noyau aplati, lenticulaire,
à chromatine
dense
formant des blocs irréguliers comme dans les cellules
canalaires.
Son cytoplasme
contient des ribosomes
et
surtout, des grains
pigmentaires sphériques très osmiophiles, denses
et homogènes. Le pôle
apical
sous-cuticulaire est garni de
microvillosités courtes et en petit nombre.
3 - Commentaires
Sur le
plan
anatomique,
l’histologie est
assez uniforme dans les trois genres étudiés
(Wendilgarda,
Theridiosoma, Naatlo ) qui diffèrent
seulement par la disposition
plus ou moins compacte de leur massif
glandulaire et la
structure pariétale de la poche
collectrice,se
singularisant chez Wendilgarda
par ses curieuses "tigettes", apophyses
de la M.E.T..
Il
en est de
même pour
la structure fine des
unités entrant dans la
constitution de
l’organe labio-sternal et qui
permettent de rattacher ses
adénocytes à la
classe 3 des
cellules glandulaires
épidermiques d’Arthropodes (Noirot
& Quennedey,1974).
Par
leur
groupement et le fait qu'elles
déversent la sécrétion dans une poche
collectrice commune, l’organe entier peut être
considéré comme “anatomiquement défini”
(Noirot & Quennedey,1974).
Les
microvillosités ont une
forme
très originale non observée dans les
autres adénocytes d’
Araignées (spermathèque
de Telema tenella
comprise) :)
en lames trapézoïdales
d’épaisseur constante et jusqu’à 10 fois plus larges
à la base qu’au sommet chez Naatlo ;
en expansions foliacées
triangulaires, parfois cordiformes, chez
Wendilgarda. Elles
évoquent celles de l’adénocyte
rétrogonoporal par leur nombre très
élevé, leur juxtaposition étroite et le fait
qu’elles semblent oblitérer la
cavité
extracellulaire. En
revanche, elles diffèrent des replis
apicaux de la spermathèque
chez
Telema
tenella (Lopez,1983b)
ainsi d'ailleurs chez les
Insectes que des
microlamelles,
également
apicales des Bathysciinae
souterrains
(Juberthie-Jupeau
&
Cazals,
1983).
Mais
c’est surtout par
le développement
remarquable de l’appareil
cuticulaire et sa poche sacciforme que l’organe
labiosternal diffère de toutes
les autres glandes prosomatiques d’ Araignées. Une
telle séparation
du réservoir et des cellules sécrétrices qui
lui
sont
annexées se rencontre en revanche fréquemment
chez
les Insectes : glande
métapleurale
des
Formicidae ( Hölldobler
&
Engel-Siegel, 1984), glandes défensives des
Coléoptères
Ténébrionidae
(Eisner
& al.,1964)ou
glandes antennaires des Pselaphidae
(De
Marzo & Vit.,1983). Néanmoins, la glande
labiosternale
présente un état de
différenciation moins poussé que chez ces Insectes
car sa poche est simple, non
compartimentée et les unités
glandulaires , dont
chacune ne comporte qu'un adénocyte,
appartiennent toutes
à un seul et même type. Elle est donc loin d'atteindre la
complexité des glandes défensives d' Hétéroptères
et surtout,
de
la glande sternale des Rhinotermitidae
(Quennedey, 1978).
Sur le plan homologique, la
glande labio-sternale pourrait être
considérée comme une variation des glandes
segmentaires d'
Aranéomorphes, sur un mode qui parait propre aux
Theridiosomatidae. Tout se passe comme si le recessus collecteur
et son
ouverture, qui siègent
normalement sur la coxa
des P I ou sur la gnathocoxe des autres
Araignées, se soient déplacés,
chez les Theridiosomatidae,
vers la ligne
médiane, en plein sternum
et plus ou moins près du labium.
Sur le plan
fonctionnel,
la présence d’un appareil terminal est en faveur de la
production d’un sémio-chimique, phéromone ou allomone ,
comme dans d’autres
glandes
tégumentaires d’Araignées. Cette
sécrétion
doit avoir
une composante glycoproteique (grand développement du Golgi,
positivité de
l'adénocyte
à
l'A.P.S.).
Elle met certainement en jeu des phénomènes
énergétiques intenses, un
métabolisme élevé (richesse du chondriome)
et des échanges
très actifs que traduit la conformation particulière des
microvillosités, ces
dernières accroissant considérablement la surface apicale
de l'adénocyte...
Il est peu probable que cette
même sécrétion soit
modifiée dans le canalicule
conducteur
car sa paroi est ininterrompue et les
cellules-enveloppes ne
présentent aucune activité
élaboratrice.
Sa résorbtion dans la
poche
pourrait expliquer l’aspect très variable du matériel qui
s’y est déposé.
En revanche, la sécrétion, si elle est phéromonale, pourrait intervenir dans la reconnaissance intra-spécifique, rôle déjà envisagé pour les glandes segmentaires rétro-gnathocoxales ou, s’il s’agit d’une allomone, dans l’attraction chimique des proies. Ces dernières, surtout des Micro-diptères Nématocères (Coddington, 1986), pourraient être alors saisies directement par l’Araignée lorsque sa toile est rudimentaire (Wendilgarda) ou s’engluer dans son piège orbiculaire à détente (Naatlo, Theridiosoma).
Note 1
: Laboratoire CNRS, Moulis
09200 : fixation des parties étudiées au
glutaraldéhyde à 2,9% dans le tampon Millonig 0,2 M, au
cacodylate pour Kaira
alba), post-fixation au tétroxyde d’osmium à 0,2% dans le
même tampon, et inclusion en épon (au Spurr pour Kaira
alba) ;
coupes fines au microtome Reichert OM U2 contrastées par
l’acétate d’uranyle, le citrate de plomb et examinées
ensuite sous 50 KV, au microscope Sopelem du Laboratoire souterrain. Travail effectué avec
Lysiane
Juberthie-Jupeau, directeur de recherches au CNRS, et ses
collaboratrices.
Note 2 :
Une fois de plus, nous
retrouvons là le caractère superficiel de telles
études et affirmations plus ou moins gratuites où
l’auteur "dérape" moins par absence de moyens techniques (d’autant plus qu’il est souvent universitaire et peut demander l’assistance d’un laboratoire de
microscopie voisin) que par manque de curiosité réelle et
méconnaissance complète de ce que peut apporter l’
histologie, moyen incomparable d’investigation pionnière.
Bibliographie
Archer, 1953.- Amer.Mus.Novitates, n°1622 (May 1953), p.1-27.
Brignoli,P.M.,1972.- Rev.suisse.Zool., 79 (1), p.361-385.
Coddington,
J.A., 1986. – Smithson.Contr.to Zoology, 422, 96 pp.
De Marzo, L. & S.Vit, 1983.-
Entomologica,18, p.77-110.
Eisner,T.,
Mc Henry,F. & M.M.Salpeter,
1964.- Journ.Morphol., 115, p.355-368.
Hölldobler,B.
& H.Engel-Siegel, 1984.- Psyche, 91, p.201-224.
Juberthie-Jupeau,L.
& M.Cazals,1983.- Mém.Biospéol.,10, p.439-444.
Quennedey, A.,1978- Thèse
Doct.Etat, Univ.Dijon, 254 pp.
Lopez,A.,1983b (avec L.Juberthie-Jupeau).-Mém.Biospéol., 10, p.413-418.
Lopez,A.,1985 (avec M.Emerit).- Mém.Biospéol.,12, p. 67-76.
Lopez,A.,1988
(avec L.Juberthie-Jupeau).- C.R.
XI e Coll.intern.europ. arachnol., Berlin, 1988, p.332-339.
Lopez,A.,1993(avec L.Juberthie-Jupeau).- Rev.Arachnol., 10 (4), 1993, p.75-92.
Lopez,A.,1994.- Bull.Soc.Sci.nat.
(Venette-Compiègne), 81 (Avril 94), p.7-15.
Noirot, Ch. & A.Quennedey, 1974.- Ann.Rev.Entomol.,19, p.61-80.
Wunderlich,J., 1980.- Verh.naturwiss.ver.Hamburg, 23 (NF), p. 255-257.

